Související příspěvek
Co učí křížové propojení RS pro proteinové komplexy o konformačních změnách
2026-02-22Cross-Linking MS pro proteinové komplexy je jedním z nejpraktičtějších způsobů, jak "zmrazit" skutečné proteinové kontakty na místě a pak je odečíst hmotnostní spektrometrií – takže se dozvíte, jak komplex mění tvar, nejen jak vypadá na jednom snímku. V Longlight Technology vidíme, že mnoho týmů začíná jednoduchou otázkou: Je můj proteinový komplex statický, nebo je důležité pro funkci přepínání mezi konformacemi? Tento článek vysvětluje začátečnickým způsobem, co vám chemické propojení spolu s hmotnostní spektrometrií (často nazývanou CL-MS nebo XL-MS) může naučit o konformačních změnách a jak proměnit výsledky v rozhodnutí, na která můžete reagovat.
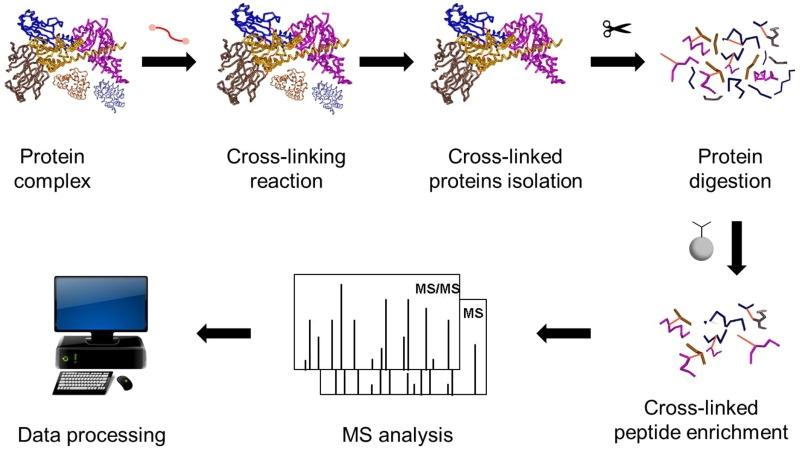
Pokroky v analýze proteinových komplexů pomocí chemického křížového síťování ve spojení s hmotnostní spektrometrií
1) Co je to křížové propojení roztroušené sklerózy?
Křížové propojení MS (často psáno XL-MS nebo CL-MS) je metoda, která vám pomáhá zjistit, které části proteinů jsou blízko u sebe – buď uvnitř jednoho proteinu, nebo mezi proteiny v komplexu – tím, že je chemicky "propojí" a poté tyto vazby identifikuje pomocí hmotnostní spektrometrie.
Tady je myšlenka v jednoduché angličtině:
• Přidat cross-linker (malý chemický "most")
Reaguje se specifickými aminokyselinami a může kovalentně spojit dva zbytky, které jsou od sebe v omezené vzdálenosti.
• Štěpit proteiny na peptidy
Enzymy (často trypsin) rozdělují bílkoviny na menší části.
• Spusť hmotnostní spektrometrii
RS detekuje peptidy, včetně křížově propojených peptidových párů.
• Analýza křížových odkazů
Každé identifikované křížové propojení se stává vzdálenostním omezením:
"Zbytek A a zbytek B byly za těchto podmínek dostatečně blízko, aby byly propojeny."
K čemu se používá
• Mapování interakcí protein–protein (PPI): kdo se koho dotýká v komplexu
• Identifikace rozhraní: které oblasti tvoří kontaktní plochu
• Konformační změna: porovnejte podmínky (APO vs ligandově vázané, mutantní vs WT), abyste viděli výskyt nebo zmizení kontaktů
• Podpora strukturálního modelování: kombinace s kryo-EM/rentgenem pro ověření nebo zdokonalení modelů
Proč je to cenné
• Může zachytit slabé nebo krátkodobé interakce (kovalentní vazba je "zmrazí")
• Často není potřeba žádné speciální označení
• Může být relativně vysokopropustný pro porovnání více podmínek
2) Proč je konformační změna tak obtížná To Zajetí
Mnoho proteinových komplexů neobstojí. Dýchají, otáčejí se, otevírají, zavírají a přeskupují podjednotky v reakci na ligandy, sůl, pH, fosforylaci nebo vazebné partnery. Tradiční konstrukční metody mohou být vynikající, ale často upřednostňují stabilní stavy. Pokud je komplex flexibilní, slabě sestavený nebo krátkodobý, můžete vidět jen část příběhu.
Propojení pomáhá, protože může kovalentně spojit dva zbytky, které přicházejí v určité vzdálenosti. Jednoduše řečeno, označuje "tyto dvě pozice byly v době reakce dostatečně blízko na kontakt". Srovnání křížových sítí vedle sebe – ligand-free vs vázané, nízko vs high salt, divoký typ vs mutant – vám řeknou, zda se komplex stlačí, rozšíří nebo rekonfiguruje.
✅ Praktický pohled pro začátečníky: konformační posuny jsou ansámblové posuny. XL-MS vidí za nejstabilnější konformaci spektrum stavů v roztoku.
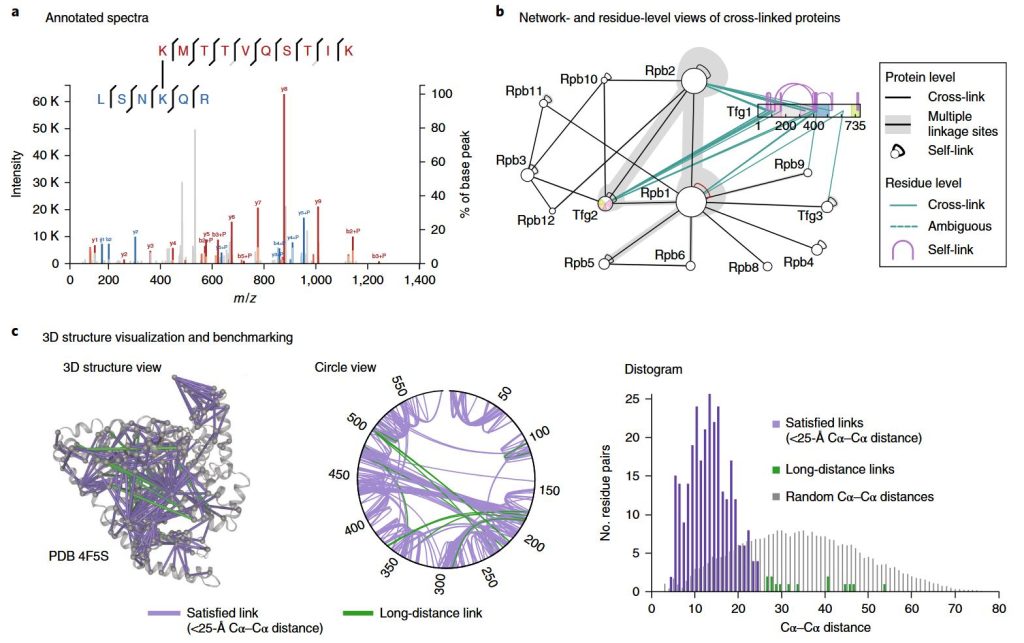
Služba křížové hmotnostní spektrometrie | MtoZ Biolabs
Jaké křížové propojení měření RS v praxi
Chemické propojení s RS kvantifikuje blízkost a interakční vzory reziduí, což je standardní přístup pro studium PPI. Křížové propojovací látky reagují s funkčními skupinami na proteinech a mohou spojit dva nebo více interagujících proteinů (nebo dvě pozice v jednom proteinu). Po propojení hmotnostní spektrometrie analyzuje propojené peptidy, což umožňuje zobrazit interakční sítě a identifikovat místa působení.
Co to znamená pro konformační změnu?
• Pokud se sada křížových vazeb objeví až po vázání ligandu, naznačuje to vznik nových kontaktů ve vázaném stavu.
• Pokud určité křížové odkazy zmizí, naznačuje to, že tyto stránky už nejsou blízko – možná se otevře komplex nebo se doména přesune.
• Pokud se křížové propojení posouvají mezi podjednotkami, může to znamenat přeskupení podjednotky nebo jinou dráhu sestavení.
✅ Co získáte touto metodou (a proč je to důležité):
• Není potřeba žádné speciální chemické označení→ můžete udržet protein blízko jeho původní formy a snížit experimentální zátěž.
• Zachycuje krátkodobé/slabé interakce → kovalentní vazby mohou zachovat kontakty, které by se jinak rozpadly během čištění nebo analýzy.
• Vysoká propustnost a rychlá rychlost analýzy → užitečné, když potřebujete efektivně porovnávat mnoho podmínek nebo konstrukcí.
• Intracelulární křížové propojení je možné → některých projektů, což vám pomůže studovat komplexy blíže jejich původnímu buněčnému kontextu, nikoli pouze in vitro.
4) Čtení "Pohyb" Z vzorů křížových spojů
Začátečníci někdy očekávají, že jeden křížový odkaz znamená jednu odpověď. V praxi však hodnota vychází ze vzorců.
Užitečný způsob, jak přemýšlet, je: křížové vazby jsou omezení vzdálenosti. Když komplex změní konformaci, změní se vzdálenost mezi dvěma zbytky. XL-MS vám nemůže vždy přesně říct úhel rotace, ale může vám říct, zda se oblasti pravděpodobně přiblížily nebo vzdálily od sebe a zda se změnila interakční mapa.
Zde jsou běžné konformační příběhy, které může XL-MS odhalit:
✅ Zhutnění vs otevření
Pokud za jedné podmínky vidíte více intraproteinových křížových spojení pokrývajících vzdálené oblasti, protein může přijímat kompaktnější stav. Pokud tyto odkazy padnou, zatímco jiné vyrostou, může se to otevírat.
✅ Přepínání rozhraní
Pokud se křížové propojení mezi podjednotkami A a B oslabí, zatímco spojení mezi A a C zesílí, naznačuje to převáženou sestavu nebo rozhraní spínač.
✅ Stabilizace ligandem nebo mutací
Ligand, který "zablokuje" konformaci, často zvyšuje reprodukovatelnost konkrétní křížové sady a snižuje smíšené vzory.
Z praktického hlediska to může vést k dalším krokům: který mutant vytvořit, kterou doménu zkrátit, která podmínka bufferu stabilizuje komplex, nebo které rozhraní ověřit jinou metodou.
5) Silnější výsledky při kombinaci XL-MS s kryo-EM nebo rentgenem
XL-MS se často používá společně s kryoelektronovou mikroskopií (cryo-EM) a rentgenovou krystalovou difrakcí pro výzkum biologické struktury. Tato kombinace je obzvlášť užitečná, když je klíčovou otázkou konformační změna.
• Kryo-EM může poskytnout strukturální model pro dominantní stavy.
• XL-MS může ověřit, zda je model konzistentní s chováním roztoku, a může označit alternativní stavy, které může být podvzorkována.
• Rentgen dokáže poskytovat domény s vysokým rozlišením, zatímco XL-MS pomáhá umístit domény do flexibilního sestavení.
✅ Praktický pracovní postup: nejprve použijte XL-MS, abyste zjistili, zda je váš komplex heterogenní. Pokud ano, můžete navrhnout podmínky, které obohacují jeden stav, než investujete do rozsáhlých investic do vysoce rozlišujících struktur.
6) Pracovní postup služeb At Longlight Technology
Mnoho laboratoří chce poznatky o Cross-Linking MS pro proteinové komplexy, aniž by si museli budovat kompletní pipeline přímo v rámci projektu. Longlight Technology podporuje jak zkušené týmy, tak nové uživatele s jasným procesem služby.
Můžete buď poslat propojené vzorky, nebo nás kontaktovat, abychom vypracovali plán propojení a poté odevzdali vzorky. Dokončujeme kompletní pracovní postup, včetně enzymového trávení, obohacení peptidů, detekce hmotnostní spektrometrie, analýzy dat a předání experimentální zprávy. Tento komplexní přístup je důležitý, protože konformační interpretace závisí na konzistentním zacházení napříč kroky.
✅ Co to znamená pro vás jako zákazníka:
• Méně chyb při předávání mezi kroky a méně "neznámých" při porovnání podmínek
• Zpráva organizovaná kolem akční interpretace, nejen surových identifikací
• Rychlejší iterace, když potřebujete testovat více konstrukcí nebo podmínek léčby
Pokud váš širší projekt zahrnuje genomiku nebo vývoj upstream testů, Longlight také poskytuje špičková genomická řešení, pokročilé laboratorní přístroje a vysoce kvalitní činidla a spotřební materiály navržené ke zvýšení efektivity a přesnosti v moderních laboratořích—podporující výzkumné postupy od molekulární biologie po přesnou analýzu.
7) Praktické CTA: Proměňte konformační otázky v testovatelné důkazy
Konformační změna není vedlejší detail. Často rozhoduje, zda je cíl opatrovatelný, zda se komplex správně sestaví a zda je mutace skutečně narušující. Cross-Linking MS pro proteinové komplexy vám poskytne důkazy, že můžete porovnávat napříč podmínkami, což vám pomůže přestat hádat a začít navrhovat.
✅ Pokud plánujete studii konformační změny, zvažte začít s jednou "srovnávací sadou":
• Apo vs. ligandem vázaný (nebo inhibitorem vázaný)
• Mutant divokého typu vs jeden rozhraní
• Jeden stabilizační pufr vs jeden stresový pufr (sůl/pH rozsah)
CTA: Pokud chcete jasný, začátečnický XL-MS plán přizpůsobený vašemu proteinovému komplexu, kontaktujte Longlight Technology a proberte svůj cíl (mapování interakcí, validace rozhraní nebo konformační porovnání). Pomůžeme vám vybrat praktickou strategii propojení a dodat interpretovatelnou zprávu, která podpoří váš další experiment – nebo váš další strukturální model.